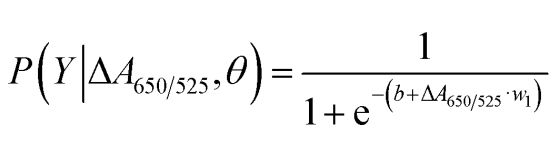Depistarea precoce a cancerului pe baza biopsiei lichide este o nouă direcție de detectare și diagnosticare a cancerului, propusă de Institutul Național al Cancerului din SUA în ultimii ani, cu scopul de a detecta cancerul în stadiu incipient sau chiar leziunile precanceroase. A fost utilizată pe scară largă ca un nou biomarker pentru diagnosticarea precoce a diferitelor tipuri de cancer, inclusiv cancerul pulmonar, tumorile gastrointestinale, glioamele și tumorile ginecologice.
Apariția platformelor pentru identificarea biomarkerilor din peisajul metilării (Methylscape) are potențialul de a îmbunătăți semnificativ screening-ul precoce existent pentru cancer, plasând pacienții în cel mai timpuriu stadiu tratabil.
Recent, cercetătorii au dezvoltat o platformă simplă și directă de detectare a peisajului de metilare, bazată pe nanoparticule de aur decorate cu cisteamină (Cyst/AuNPs), combinate cu un biosenzor bazat pe smartphone, care permite screening-ul precoce rapid al unei game largi de tumori. Screening-ul precoce pentru leucemie poate fi efectuat în termen de 15 minute de la extracția ADN-ului dintr-o probă de sânge, cu o precizie de 90,0%. Titlul articolului este Detectarea rapidă a ADN-ului canceros în sângele uman utilizând AuNPs acoperite cu cisteamină și un smartphone cu învățare automată.
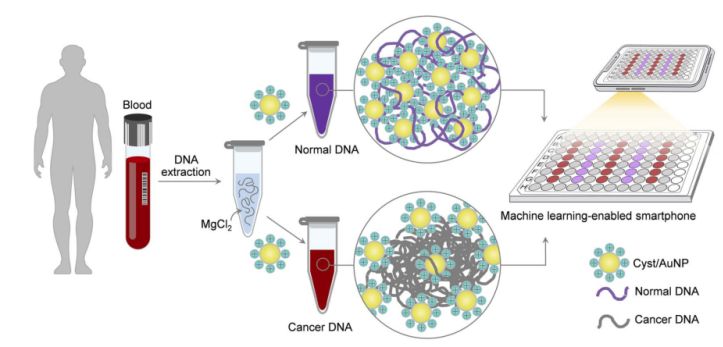
Figura 1. O platformă simplă și rapidă de detectare a cancerului prin intermediul componentelor Cyst/AuNPs poate fi realizată în doi pași simpli.
Acest lucru este prezentat în Figura 1. Mai întâi, s-a utilizat o soluție apoasă pentru a dizolva fragmentele de ADN. Apoi, în soluția amestecată s-au adăugat nanoparticule de chist/AuNP. ADN-ul normal și cel malign au proprietăți de metilare diferite, rezultând fragmente de ADN cu modele de autoasamblare diferite. ADN-ul normal se agregă liber și, în cele din urmă, agregă nanoparticule de chist/AuNP, ceea ce duce la natura deplasată spre roșu a nanoparticulelor de chist/AuNP, astfel încât o schimbare de culoare de la roșu la violet poate fi observată cu ochiul liber. În schimb, profilul unic de metilare al ADN-ului canceros duce la producerea unor clustere mai mari de fragmente de ADN.
Imaginile plăcilor cu 96 de godeuri au fost realizate folosind camera unui smartphone. ADN-ul canceros a fost măsurat cu un smartphone echipat cu învățare automată, comparativ cu metodele bazate pe spectroscopie.
Screeningul cancerului în probe de sânge real
Pentru a extinde utilitatea platformei de detectare, cercetătorii au aplicat un senzor care a reușit să distingă între ADN-ul normal și cel canceros în probele de sânge reale. Modelele de metilare la situsurile CpG reglează epigenetic expresia genelor. În aproape toate tipurile de cancer, s-a observat că modificările în metilarea ADN-ului și, prin urmare, în expresia genelor care promovează tumorogeneza se alternează.
Ca model pentru alte tipuri de cancer asociate cu metilarea ADN-ului, cercetătorii au folosit probe de sânge de la pacienți cu leucemie și de la persoane sănătoase din grupul de control pentru a investiga eficacitatea peisajului de metilare în diferențierea cancerelor leucemice. Acest biomarker al peisajului de metilare nu numai că depășește metodele existente de screening rapid pentru leucemie, dar demonstrează și fezabilitatea extinderii la detectarea precoce a unei game largi de tipuri de cancer folosind acest test simplu și direct.
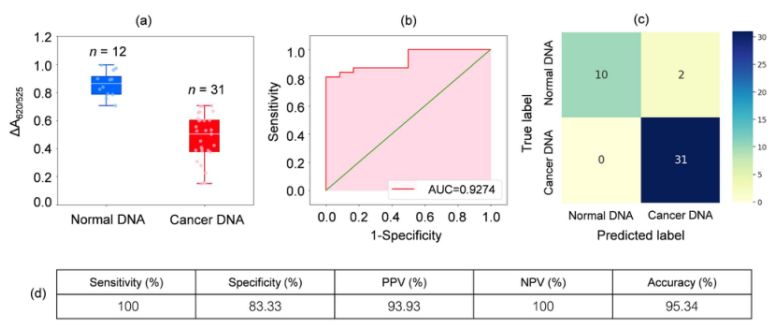
A fost analizat ADN-ul din probe de sânge de la 31 de pacienți cu leucemie și 12 persoane sănătoase. După cum se arată în diagrama tip box din Figura 2a, absorbanța relativă a probelor de cancer (ΔA650/525) a fost mai mică decât cea a ADN-ului din probele normale. Acest lucru s-a datorat în principal hidrofobicității sporite, ceea ce a dus la o agregare densă a ADN-ului canceros, ceea ce a împiedicat agregarea nanoparticulelor chistice/AuNP. Drept urmare, aceste nanoparticule au fost complet dispersate în straturile exterioare ale agregatelor canceroase, ceea ce a dus la o dispersie diferită a nanoparticulelor chistice/AuNP adsorbite pe agregatele de ADN normal și canceros. Curbele ROC au fost apoi generate prin variația pragului de la o valoare minimă de ΔA650/525 la o valoare maximă.
Figura 2.(a) Valorile relative ale absorbanței soluțiilor de chisturi/AuNP care arată prezența ADN-ului normal (albastru) și canceros (roșu) în condiții optimizate
(DA650/525) a diagramelor box; (b) Analiza ROC și evaluarea testelor de diagnostic. (c) Matricea de confuzie pentru diagnosticul pacienților normali și cu cancer. (d) Sensibilitate, specificitate, valoare predictivă pozitivă (VPP), valoare predictivă negativă (VPN) și acuratețea metodei dezvoltate.
După cum se arată în Figura 2b, aria de sub curba ROC (AUC = 0,9274) obținută pentru senzorul dezvoltat a prezentat o sensibilitate și specificitate ridicate. După cum se poate observa din diagrama box plot, cel mai de jos punct care reprezintă grupul de ADN normal nu este bine separat de cel mai înalt punct care reprezintă grupul de ADN canceros; prin urmare, s-a utilizat regresia logistică pentru a diferenția între grupurile normale și cele canceroase. Având în vedere un set de variabile independente, aceasta estimează probabilitatea apariției unui eveniment, cum ar fi un grup canceros sau normal. Variabila dependentă variază între 0 și 1. Prin urmare, rezultatul este o probabilitate. Am determinat probabilitatea de identificare a cancerului (P) pe baza ΔA650/525 după cum urmează.
unde b=5,3533,w1=-6,965. Pentru clasificarea eșantioanelor, o probabilitate mai mică de 0,5 indică o eșantion normală, în timp ce o probabilitate de 0,5 sau mai mare indică o eșantion cu cancer. Figura 2c prezintă matricea de confuzie generată din validarea încrucișată de tip „leave-it-alone”, care a fost utilizată pentru a valida stabilitatea metodei de clasificare. Figura 2d prezintă pe scurt evaluarea testului de diagnostic al metodei, inclusiv sensibilitatea, specificitatea, valoarea predictivă pozitivă (VPP) și valoarea predictivă negativă (VNP).
Biosenzori bazați pe smartphone-uri
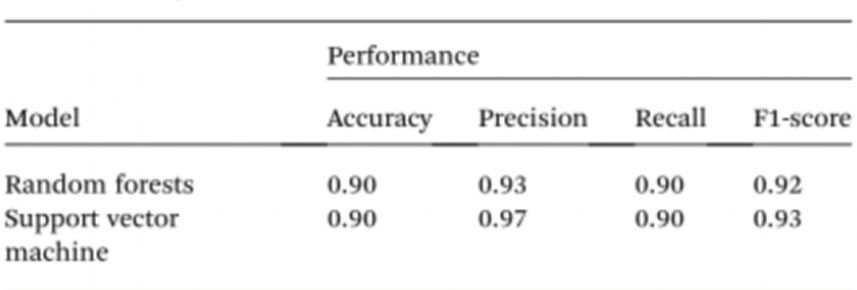
Pentru a simplifica și mai mult testarea probelor fără utilizarea spectrofotometrelor, cercetătorii au folosit inteligența artificială (IA) pentru a interpreta culoarea soluției și a distinge între indivizii normali și cei canceroși. Având în vedere acest lucru, viziunea computerizată a fost utilizată pentru a traduce culoarea soluției de Cyst/AuNPs în ADN normal (violet) sau ADN canceros (roșu), utilizând imagini ale plăcilor cu 96 de godeuri preluate cu ajutorul camerei unui telefon mobil. Inteligența artificială poate reduce costurile și poate îmbunătăți accesibilitatea în interpretarea culorii soluțiilor de nanoparticule, fără utilizarea niciunui accesoriu hardware optic pentru smartphone. În cele din urmă, două modele de învățare automată, inclusiv Random Forest (RF) și Support Vector Machine (SVM), au fost antrenate pentru a construi modelele. Atât modelul RF, cât și cel SVM au clasificat corect probele ca pozitive și negative, cu o precizie de 90,0%. Acest lucru sugerează că utilizarea inteligenței artificiale în biosenzorizarea bazată pe telefoane mobile este destul de posibilă.
Figura 3. (a) Clasa țintă a soluției înregistrată în timpul pregătirii probei pentru etapa de achiziție a imaginii. (b) Imagine exemplu realizată în timpul etapei de achiziție a imaginii. (c) Intensitatea culorii soluției de chist/AuNPs din fiecare godeu al plăcii cu 96 de godeuri extrasă din imagine (b).
Folosind Cyst/AuNPs, cercetătorii au dezvoltat cu succes o platformă simplă de detectare a peisajului de metilare și un senzor capabil să distingă ADN-ul normal de ADN-ul canceros atunci când utilizează probe de sânge real pentru screening-ul leucemiei. Senzorul dezvoltat a demonstrat că ADN-ul extras din probe de sânge real a fost capabil să detecteze rapid și eficient din punct de vedere al costurilor cantități mici de ADN canceros (3nM) la pacienții cu leucemie în 15 minute și a prezentat o precizie de 95,3%. Pentru a simplifica și mai mult testarea probelor prin eliminarea necesității unui spectrofotometru, s-a utilizat învățarea automată pentru a interpreta culoarea soluției și a diferenția între indivizii normali și cei canceroși folosind o fotografie făcută cu telefonul mobil, iar precizia a putut fi, de asemenea, atinsă la 90,0%.
Referință: DOI: 10.1039/d2ra05725e
Data publicării: 18 februarie 2023
 中文网站
中文网站